Hg2I2 → Hg2^2+ + 2I^-. Hg2^2+의 구조
왜 I^-의 몰수는 Hg2^2+의 몰수의 2배인가?
[참고] Mercury(I) chloride의 화학식은 왜 Hg2Cl2인가?
[ https://ywpop.tistory.com/12488 ]
Hg2^2+ 가
Ca^2+ 처럼,
1개의 이온으로 존재하기 때문입니다.
[그림] The structure of mercury(I) ion, Hg2^2+.
이 때문에
CaI2 → Ca^2+ + 2I^-
Ca^2+ : I^- = 1 : 2 계수비(= 몰수비)
이듯이,
Hg2I2 → Hg2^2+ + 2I^-
Hg2^2+ : I^- = 1 : 2 계수비(= 몰수비)
이므로,
I^-의 몰수는 Hg2^2+의 몰수의 2배.
[키워드] 수은 기준, 수은 이온 기준, Hg2^2+ 기준, Hg2^2+ 사전, Hg2^2+ dic, Hg2^2+ 이온 기준, Hg2^2+ 이온 사전

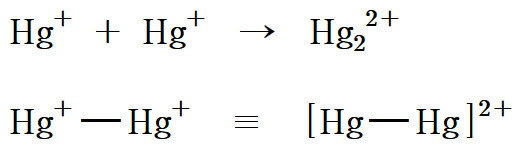
YOU MIGHT LIKE
모두 보기댓글 쓰기